GB 4789.2-2016 食品安全国家标准 食品微生物学检验 菌落总数测定 01 稀释度的选择 液体样品可直接取原液进行检验;固体或者半固体则必须依据检验经验,选取2-3个适宜稀释度进行检验(
GB 4789.2-2016
液体样品可直接取原液进行检验;固体或者半固体则必须依据检验经验,选取2-3个适宜稀释度进行检验(一般样品选取1:10,1:100,1:1000三个稀释度进行检验。若遇到不常做的样品,可适当延长稀释度至1:10000甚至更大)。
分别吸取1mL灭菌生理盐水到平皿中做空白对照,若空白有菌落生长则该实验无效。
根据对样品污染情况的估计,若样品有表面蔓延生长的可能性,则待第一次倾注的琼脂凝固后,可在表面再覆盖一层琼脂以避免菌落蔓延而难以计数。
本标准的难点在于菌落计数及计算。
1)菌落计数时,从低稀释度的平板开始计数。若所有平板上的菌落数均小于30CFU,则需计数所有平板上的菌落数,但仅采用最接近30CFU的两个平板的菌落数来计算最终菌落数。
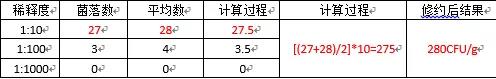
2)当第一稀释梯度一个板上菌落数高于30,另一个低于30,则依据标准应当以介于30-300之间的菌落数作为该稀释梯度的菌落数。

3)若所有平板上的菌落数均大于30CFU,则只计数30-300CFU之间的平板上的菌落数,并采用这些数据,依据标准中给出的公式,进行最终菌落总数的计算,此时将大于300CFU的记为“多不可计”,以TNTC表示。

4)若所有稀释度的平均菌落数都大于300,则不能所有都记为TNTC,必须将最高稀释度的两个平板上的菌落数逐一的计数,再计算平均数,该平均数为该梯度的菌落总数,其余平板上的菌落数可记为TNTC。

5)若所有平板均无菌落生长,则以小于1乘以最低稀释倍数。
注意:对于该情况,一直存在争议,不同的检验人员可能做法不一,有人保留为5CFU,有人保留为10CFU,并无固定做法,建议实验室保持一贯做法,不要随意更改。
GB 4789.15-2016
1)孟加拉红培养基灭菌条件比较特殊:121℃,20min;
2)稀释液可选择生理盐水、硝酸盐缓冲液,还可以选择无菌水;
3)正置平板培养。未避免孢子扩散、菌落蔓延,可选择使用一次性塑料培养皿;
4)“观察并记录培养至第5d的结果”,意味着需要从培养的第二天开始逐日观察并记录霉菌和(或)酵母的生长情况,且原始记录须体现“逐日观察”;
GB 4789.3-2016
建议新手们认真按照标准进行证实实验,此证实实验操作简单,每一次VRBA上有菌落生长都进行证实实验,如此往复3-4次,对于哪种形态才是大肠菌群均可了然于心。
选取15-150CFU之间的平板,挑选可疑菌落进行证实实验。举例如下:
注意:A. 每种可疑菌落挑取5个,每个菌落放入1根GBLB管中;B. “产气者,记为大肠菌群阳性管‘’,就要求在实验前必须认真筛选BGLB管,凡产气的GBLB管应弃去不用。
选取适宜菌落数的平板挑取菌落进行证实试验,若证实全部为阴性,则需要再挑取更低稀释度的平板上的菌落,建议可疑和典型菌落分别挑取10个进行验证试验,若第二次证实实验均呈阴性,以<1乘以最低稀释度进行计算。
来源:食品论坛网友转载分享


Copyright 2015-2016 山西山阳生物药业有限公司 版权所有 晋ICP备18010233号-1 互联网药品信息服务(苏)-非经营性-2013-0066